Connu pour son utilisation dans les thermomètres, le Mercure est un métal mi-liquide mi-solide hautement toxique pour l’organisme. Quels sont les effets d’une intoxication à ce métal ? Quels sont les différents facteurs de risque à l’empoisonnement ? Quels sont les symptômes de l’intoxication ? Apprenez à connaitre à travers cet article ce métal et ses effets sur l’organisme d’après la science. Ceci est un simple résumé d’études qui ne peut remplacer les avis des spécialistes.

Appelé « vif-argent » jusqu’au XIXème siècle, le mercure est le seul métal qui se présente sous format liquide lorsqu’il est soumis dans des conditions normales de température et de pression. Longtemps, cet élément chimique fut utilisé dans les thermomètres avant d’être retiré du marché en 1998, en raison de sa haute toxicité. La vente d’objets le contenant ainsi qu’un nombre important de ses usages sont devenus interdits, depuis la découverte de ses effets néfastes sur la santé. Le mercure est à la fois écotoxique, toxique et reprotoxique, que ce soit sous sa forme liquide, de sels – cinabre et calomel – ou bien organométallique, telle que le monométhylmercure et le diméthylmercure. L’intoxication à cet élément est connu sous les termes scientifiques de hydrargyrie, hydragisme ou encore hydragyrisme.
Sommaire
Présentation du mercure
Recherches et découvertes
Avant XIXème, en 1987 plus précisément ; deux dénominations furent utilisées concurremment pour appeler ce corps chimique, à savoir vif-argent et mercure. C’est la normalisation de la nomenclature chimique qui a imposé le nom de « mercure », à compter de cette date.
Ce métal mi-liquide mi-solide n’a fait aucun objet d’une découverte particulière. Ses premières utilisations remontent pas mal de siècles avant J–C. Le premier ouvrage scientifique ayant parlé de cet élément date de l’an -371, écrit par le savant grec Théophraste. Ce scientifique parla dans ses écrits de son extraction en broyant du cinabre avec un pilon d’airain et du vinaigre. Rappelons que le cinabre n’est autre que le minerai dans lequel il se présente naturellement, α-HgS ou sulfure de mercure.
Propriétés physiques et chimiques

Le mercure a comme numéro atomique le 80 et symbole Hg. Cet élément chimique possède 38 isotopes, dont la plupart sont stables pouvant être utilisés dans les traçages isotopiques, ainsi qu’instables et radioactifs. L’isotope 203 Hg, par exemple, est synthétisé à partir des retraitements de déchets nucléaires ou bien produit par les centrales nucléaires. Sa période radioactive atteint les 46,59 jours et son activité massique est de l’ordre de 5,11.10 à la puissance 14 Bq.g-1. (1)
Dans la nature, ce métal se présente sous diverses formes, corps simple, vapeur monoatomique et composés, notamment sous forme de sulfures (sulfure de mercure ou HgS) et quelque fois de chlorures ou d’oxydes. Le corps simple est liquide, de couleur grise brillante, avec une densité élevée de l’ordre de 13,6 et très mobile. Sa température de solidification est de -39°C. On le retrouve surtout dans les terres volcaniques, puisqu’il provient des volcans. Côté propriété chimique, cet élément ne réagit pas dans les acides aqueux.
Propriétés biologiques
Le mercure n’a aucun rôle particulier dans l’organisme humain. Ce n’est pas un oligo-élément. Il est tout simplement toxique pour l’Homme, quelle que soit sa forme. Il est important de noter que les effets de ce métal se différencient en fonction de sa forme : les composés organiques à l’instar du méthylmercure CH3Hg sont plus toxiques que les formes ionisées tels que le Hg+ et Hg++. La vapeur monoatomique du mercure est hautement toxique et plus dangereuse, car plus facile à assimiler par l’organisme par simple inhalation. Ce métal a pourtant tendance à s’accumuler et est très faiblement éliminé par l’organisme.
Les autorités sanitaires ont établi des doses limites à ne pas dépasser, qui varient d’un pays à l’autre. En 2003, l’OMS a fixé un DHTP, ou dose hebdomadaire totale provisoire, de l’ordre de 1,6 μg meHg/kg mc/sem. En France, la quantité maximale de méthylmercure admise est de 3,3 μg meHg/kg mc/sem d’après l’AFSSA, alors qu’aux États-Unis celle-ci est de 0,7 μg meHg/kg mc/sem. (3)
Études toxicologiques du mercure
Ce métal a-t-il un effet cytotoxique ?
Le mercure fait partie intégrante des métaux toxiques non biodégradables qui ont des effets néfastes sur les êtres vivants, Homme, animaux et végétaux. Cette revue scientifique publiée en 2000 a répertorié les différents essais cliniques qui ont étudié la relation entre ces métaux et le fonctionnement des cellules.
Utilisé chez des modèles animaux, le mercure conduit à l’apoptose des cellules, induit des aberrations chromosomiques ou favorise des cancers. La mort cellulaire programmée ne peut pourtant se produire que lorsque les dommages cellulaires ou bien les dommages du matériel génétique dépassent largement la capacité de régénération de la cellule. (4)
Est-il capable de favoriser l’altération de la fonction cognitive ?

Le mercure Hg est l’un des principaux contaminants environnementaux qui préoccupent les scientifiques actuellement. En effet, ce métal, lorsqu’il se retrouve dans un milieu aquatique et ce indépendamment de sa forme initiale – organique ou inorganique – se transforme en méthylmercure MeHg encore plus toxique, via un processus de méthylation. Cette publication a parlé du phénomème de bioaccumulation de ce métal dans la chaine alimentaire et de ses effets sur la fonction cognitive. Ce phénomène de méthylation dont il est question ici s’effectue par le biais des micro-organismes, tels que les planctons, qui seront pourtant la nourriture principale des petits-poissons. Ces derniers seront eux-mêmes les proies des poissons plus gros, qui entrent dans la liste des aliments consommés par l’Homme.
Cette revue scientifique a souligné que l’absorption de ce métal lipophile via le système gastro-intestinal est à hauteur de 95 %. Le MeHg ingéré se retrouve donc rapidement dans le sang et affecte les différents organes. Il a été remarqué que les nourrissons, les enfants de bas-âges et les fœtus exposés fréquemment à ce métal via leurs alimentations et ou leur environnement ont des problèmes de développement au niveau de leurs cerveaux. Les enfants nés des mères fréquemment exposées au mercure souffrent de dysfonctions cérébrales, comprenant retard mental, convulsions, ataxie cérébrale, et troubles psychomoteurs. (5)
Peut-il entrainer la dégradation du système visuel ?
Très peu d’études scientifiques ont parlé de l’effet de ce métal sur les systèmes visuel et auditif, alors que les premiers signes de l’intoxication concernent surtout ces fonctions de l’organisme. Il a été démontré lors de l’incident d’intoxication en Irak et au Japon que le cortex visuel est particulièrement vulnérable lors d’une exposition aiguë au méthylmercure. D’importantes lésions ont été remarquées chez les victimes de la tragédie de Minamata en 1949, entrainant cécité bilatérale, vision tunnel, constriction du champ visuel, ou encore faible vision de nuit. (6)
Une exposition chronique à une dose plus réduite de ce métal a entrainé de son côté des dysfonctions visuelles, telles que perte du champ visuel périphérique, sensibilité aux contrastes et diminution de la capacité à identifier les couleurs. Ces cas ont été notés chez des dentistes qui sont exposés à la vapeur de mercure au quotidien, dégagée par les amalgames dentaires utilisés en traitement. (7)
Facteurs de risque et symptômes de l’intoxication au mercure
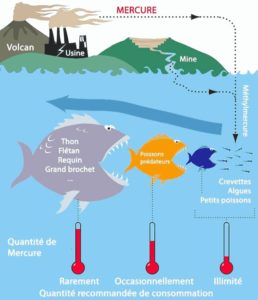
Les principaux facteurs augmentant les risques d’intoxication au mercure demeurent :
– La fréquentation des sites d’orpaillage ;
– L’exploitation de ce métal et de ses composés ;
– La consommation de poissons, d’eau et de semences contaminés ;
– L’usage d’amalgames dentaires. Ce sont les premières sources d’exposition à cet élément chimique en France ;
– L’usage de certains produits cosmétiques de mauvaise qualité et irrespectueux des normes d’hygiène et de sécurité, utilisant du mercure comme agent conservateur ;
– L’utilisation de thermomètre et de tensiomètre à mercure. La vente de ces matériels sont interdits depuis 1998, mais certains foyers en possèdent encore actuellement ;
– Certains vaccins avec conservateur mercuriel ;
– L’utilisation d’ampoule fluorescente, qui renferme en moyenne 3mg de Hg.
Les symptômes de l’intoxication au mercure dépendent de son type – chronique ou aigu – et de son mode d’absorption, par ingestion ou inhalation. Des signes, tels que irritation des voies respiratoires, gonflement du poumon, cécité, trouble du langage, perte de mémoire, dysfonctionnement cérébral, perturbation du système endocrinien, lésion des organes dont notamment les reins et le foie, sont notés chez le sujet intoxiqué. Seul l’établissement d’un profil lipidique permet de déterminer s’il s’agit réellement d’une intoxication au Hg.
Références
(1) Beaugelin-Seiller & O. Simon. Fiche pédagogique Radionucléide 203Hg IRSN. 21 pp, 2004-05-12.
(2) Article de la revue du BRGM sur le mercure et la santé.
(3) Jean-Paul Bourdineaud, Dossier : « Populations citadines pas assez protégées de la contamination de mercure via la consommation de poissons », 18 mai 2015.
(4) Waalkes et al. « Metals and disorders of cell accumulation: modulation of apoptosis and cell proliferation » Toxicological Sciences 56.2 (2000): 255-261.
(5) Saint-Amour D et al. « Contribution des neurosciences cognitives pour l’étude de l’impact des contaminants environnementaux sur le développement des fonctions cérébrales ». Revue de neuropsychologie 2002, 4(3), 163-173.
(6) Bakir F et al. « Methylmercury poisoning in Iraqi children : clinical observations over two years. Br Med J1978;1:6113613-616.
(7) Canto-Peirera LHM et al. « Visual impairmenton dentist related to occupation mercury exposure ». Environ Toxicol Pharmacol 2005;19:3517-522.



