Le NAD+ est depuis un certain temps l’objet de concentration de nombreux scientifiques désireux de trouver une solution efficace et sûre pour lutter contre les maladies dégénératives liées à l’âge et prolonger l’espérance de vie humaine. L’intérêt porté pour cette molécule ne cesse de grandir jour après jour, notamment depuis la publication de l’étude menée par David Sinclair et ses collègues américains et australiens. Mais de quoi il s’agit réellement ? Et comment peut-elle nous aider à rester longtemps jeunes et en bonne santé ? Ce billet dévoile les secrets du NAD+ et ses bienfaits selon la science. Attention, ces informations ne doivent pas être considérées comme un avis medical.
Sommaire
Ce qu’il faut connaitre sur cette molécule
Avant de parler des bienfaits de cette molécule pour l’organisme, de sa biosynthèse et des dangers liés à sa perte, il convient dans un premier temps de définir ce que c’est réellement.
– Le NAD est, en fait, l’abréviation donnée à la coenzyme, dite Nicotinamide Adénine Dinucléotide, visible dans toutes les cellules vivantes. Ce composé est un dinucléotide, du fait de la présence de deux nucléotides reliés par des groupes phosphates dans sa structure. Chacun de ces nucléotides comprend une base d’adénine et un nicotinamide.
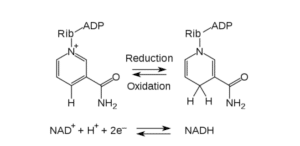
Le NAD se décline en deux formats, dont l’un réduit dit NADH et l’autre oxydé NAD+. De nombreux processus métaboliques et biologiques de l’organisme humain se reposent sur la présence de cette molécule.
– Le NAD+, comme il a été dit, est la forme oxydée du NAD ou oxydant. Cette molécule joue le rôle de cofacteur dans de nombreux processus biologiques liés à la santé et à la longévité, tels que dans la réparation de l’ADN et le bon fonctionnement des mitochondries. Elle se charge du transfert d’électrons au cours des réactions d’oxydoréduction (réactions chimiques pendant lesquelles il y a échange d’électrons entre l’oxydant et le réducteur). Malheureusement, sa synthèse diminue progressivement avec l’âge ; ce qui cause un dysfonctionnement non négligeable au niveau des cellules et de l’activité de certaines enzymes qui en dépendent, telles que les sirtuines 1 à 7 (une classe de protéines enzymatiques responsables de la régulation d’informations au sein des cellules).
– La forme réduite NADH, de son côté, agit comme un agent réducteur ou donneur d’électrons. Ce composé peut retrouver sa forme NAD+ lors de la voie de sauvetage du NAD, pendant la réaction d’oxydoréduction.
> À noter que, l’équilibre entre ces deux formes de NAD est vraiment important, car il permet de déterminer le niveau d’activité métabolique et de la santé des cellules, ainsi que de son état redox. Celui-ci peut être évalué par un rapport entre le NAD+ et NADH. (1)
Un élément clé dans différents processus biologiques
Maintenir son taux à un niveau supérieur est essentiel non seulement pour rester en bonne santé, mais également pour garantir le bon déroulement des différents processus biologiques. Les maladies dégénératives qui affectent la génération actuelle et la baisse de l’espérance de vie sont, en effet, liées à la perturbation des différentes fonctions de l’organisme.
– Cette forme oxydée du NAD joue, par exemple, le rôle de substrat dans la production de SIRT1 qui se trouve dans la liste des gènes suppresseurs de tumeurs, ainsi que d’autres sirtuines qui sont essentiels au bon déroulement de divers processus, comme les réactions inflammatoires, l’apoptose cellulaire, la biogenèse des mitochondries ou encore la restriction énergétique.
– Cette molécule est aussi nécessaire à la résistance au stress et la réactivité de l’organisme en cas de stress oxydatif, une cause connue du vieillissement prématuré des cellules et de la dégradation des tissus.
– La maintien de l’intégralité et la réparation de l’ADN reposent aussi sur cette forme oxydée du NAD. Sa présence est, en effet, indispensable pour les transferts d’électrons au niveau des mitochondries. Autrement dit, cette molécule garantit la continuité des réactions chimiques qui se produisent dans les cellules. C’est le dérèglement de ce processus qui conduit à la formation d’un cancer.
Augmenter le taux de NAD+ pour une santé de fer et la longévité
Depuis déjà un certain temps, un nombre important de scientifiques essaient de trouver des solutions pour augmenter naturellement le taux de NAD+ dans l’organisme, afin de lutter contre les maladies dégénératives et d’augmenter l’espérance de vie. Différentes techniques ont été adoptées pour ce faire, pour ne citer que celles qui permettent d’améliorer sa biosynthèse et celles qui inhibent l’activité des enzymes qui le consomment.

Avant de découvrir les bienfaits thérapeutiques apportés par un NAD+ élevés, parlons un peu de sa synthèse naturelle. Sa production au sein de l’organisme se fait de deux façons, soit par voie de novo qui fait intervenir des précurseurs élémentaires dont les principaux sont le tryptophane, l’acide nicotinique et le nicotinamide, soit par voie de sauvetage ou récupération, qui consiste en un recyclage de ce coenzyme par le biais de ses deux formes oxydées et réduites. (2)
Le NAD+ est-il capable de favoriser l’homéostasie cellulaire et augmenter la durée de vie ?
Des publications ont mis en évidence le pouvoir du NAD+ à favoriser et maintenir l’homéostasie cellulaire, c’est-à-dire la capacité de la cellule à conserver l’équilibre de ses différentes fonctions malgré la variation de son environnement. Les auteurs de ces études ont constaté que le niveau de cette molécule est particulièrement bas chez les souris âgées et les vers du genre C.elegans expérimentés. L’administration de produits précurseurs de NAD+ et inhibiteurs de PPAR (récepteurs nucléaires activés par les proliférateurs de peroxysomes qui participent au métabolisme des acides gras et à l’inflammation) chez ces sujets a permis de rétablir l’équilibre protéique, d’empêcher le déclin métabolique, de stimuler l’activité des mitochondries et de prolonger leur durée de vie. (3)
Pour l’instant, la plupart des essais cliniques ont été réalisés sur des modèles animaux. Ce qui ne nous permet pas de confirmer la réelle efficacité de ces produits précurseurs de NAD+ sur l’homme.
Ce composé peut-il améliorer la sensibilité à l’insuline ?
Certains chercheurs ont aussi prouvé qu’un taux élevé de NAD+ permet de lutter contre le diabète, voire le traiter, en améliorant la sensibilité à l’insuline. Il a été constaté lors des différentes expériences réalisées que la biosynthèse de cette molécule est inhibée par l’enzyme dite nicotinamide phosphoribosyltransférase qui est surexprimée chez les sujets diabétiques et ceux qui consomment des aliments trop riches en graisses. Chez un groupe de souris diabétiques de type 2, l’administration de nicotinamide mononucléotide (NMN), un précurseur direct, a permis d’améliorer l’intolérance au glucose et le profil lipidique, ainsi que d’activer le SIRT1. (4)
D’autres essais cliniques demeurent toutefois nécessaires avant de confirmer cette qualité thérapeutique. La plupart des observations ont été en effet menées sur des modèles animaux. Ce qui ne nous permet pas de conclure sur quoi que ce soit pour l’instant.
Est-ce une solution pour prévenir les maladies dégénératives liées à l’âge ?
Comme il a été mentionné précédemment, le NAD+ est un substrat essentiel dans la synthèse des sirtuines, en particulier des SIRT1 et SIRT3, les plus observés des scientifiques. C’est un élément précieux pour la régulation et la fonction de ces protéines enzymatiques.
Ce n’est pas tout, l’activation de la SIRT1 et de la SIRT3, en améliorant le niveau de NAD+ grâce à l’administration de nicotinamide riboside, a permis chez les souris de laboratoires de prévenir les troubles métaboliques, dont l’obésité et le diabète de type 2, dus à un régime trop riche en graisses. (5)
Dans une autre revue scientifique, il a été lu que la surexpression de SIRT1 et de SIRT3 liée à l’amélioration de NAD+ a atténué les modifications physiopathologiques liées au vieillissement et protégé les sujets testés contre le développement de différentes maladies dégénératives, comme le diabète, les cancers, les maladies inflammatoires, et les troubles de la cognition. La même publication a même mentionné dans ses lignes que le SIRT1 prévient le dépôt de plaques séniles ou amyloïdes sur le tissu nerveux, la cause de la maladie d’Alzheimer (2). Des propriétés médicinales intéressantes qui nécessitent toutefois encore plus d’études cliniques sur l’homme. Les expériences menées sur ces animaux de laboratoire ne suffisent pas, bien que les résultats soient encourageants.
Consommateurs de NAD+
Normalement, le NAD+ est conservé grâce à son cycle de sauvetage. Son niveau diminue, néanmoins, avec l’âge et à cause des différents processus vitaux de l’organisme qui ont besoin de son intervention en tant que substrat.
Parmi les plus grands consommateurs, il y a les :
– PPARP : ce sont ces récepteurs nucléaires qui diminuent fortement le niveau de NAD+ dans l’organisme, en particulier chez les sujets âgés où le besoin de réparation d’ADN est important. Bloquer les PPAR semble une bonne stratégie pour augmenter le taux de NAD+.
– Sirtuines : Ces protéines enzymatiques figurent aussi parmi les plus gros consommateurs de NAD+ car leurs synthèses et fonctions en dépendent entièrement.
– CD38 : Cette enzyme localisée surtout au niveau du paroi cellulaire consomme aussi une quantité non négligeable de NAD+ pour assurer son rôle. Celle-ci intervient dans l’homéostasie du calcium cellulaire. Des rapports scientifiques ont parlé des effets bénéfiques liés à l’inhibition de son activité, tels que la possibilité de traiter les troubles métaboliques.
Références
(1) Freya Q et al. « Environnement rédox de la cellule vu à travers l’état rédox du couple disulfure / glutathion glutathion », Biologie et médecine des radicaux libres, vol 30, n ° 11, juin 2001, p.1191-1212.
(2) Sergio P et al. « Dissection du contrôle systémique du métabolisme et du vieillissement dans le monde NAD: L’importance de la biosynthèse de NAD médiée par Sirt1 et NAMPT ». Dpt of Dev Biology, États-Unis d’Amérique, 28 mars 2011.
(3) Laurent M et al. « La voie NAD + / sirtuine module la longévité par l’activation de la signalisation mitochondriale UPR et FOXO ». Cellule, 18 juillet 2014.
(4) Yoshino J et al. « Le mononucléotide nicotinamide, un intermédiaire clé de la NAD (+), traite la physiopathologie de l’alimentation et du diabète induit par l’âge chez la souris ». Cell Metab 2011 oct 5; 14 (4): 528-36.
(5) Canto C et al. « Le nicotinamide riboside, précurseur de NAD +, stimule le métabolisme oxydatif et protège contre l’obésité induite par un régime alimentaire riche en graisses ». Cell Metab, 6 juin 2012; 15 (6): 838-47.