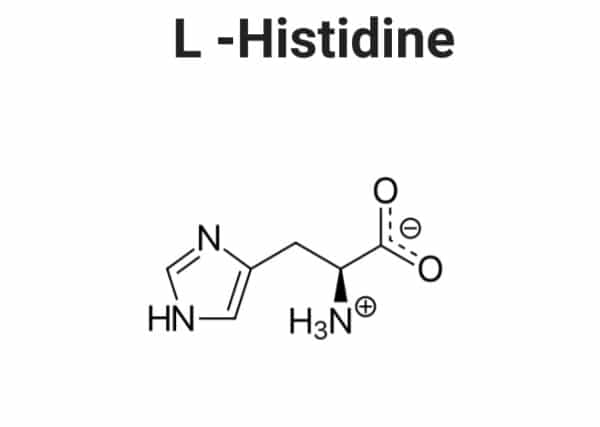
Acide aminé non essentiel pouvant être produit par l’organisme et essentiellement présent dans la spiruline, l’Alanine possède des bienfaits santé appréciables. Lesquels ? Quelle est la différence entre Alanine et β-alanine ? Comment bien choisir son complément ? Ce billet présente les particularités de cet acide aminé et ses propriétés médicinales selon la science. Soulignons que ces informations ne remplacent pas les conseils d’un professionnel de santé.
Sommaire
L’alanine figure parmi les 13 acides aminés non essentiels, car l’organisme est capable de la synthétiser naturellement. Cet acide α-aminé est fréquemment retrouvé dans les protéines du fait que son énantiomère L, L ou S (+)-alanine, est un acide aminé protéinogène. Le terme protéinogène, comme nous l’avons déjà vu dans d’autres articles sur les acides aminés, est utilisé pour désigner les acides aminés incorporés dans les protéines. Autrement dit, c’est le type d’acide aminé qui entre dans la fabrication de protéines. Il peut se lier à ces derniers au moment de la traduction de l’ARN messager par les ribosomes. Ceux qui ne le peuvent pas sont dits non-protéinogènes. Cet acide aminé est codé génétiquement par les codons commençant par GC.
Présentation de l’alanine
Propriétés physiques et chimiques
L’alanine a été découverte et synthétisée pour la première fois en 1850 par le scientifique allemand Adolph Strecker. Elle est connue sous les abréviations scientifiques Ala, A ou le nom Acide 2-aminopropanoïque. Sa dénomination est tirée du mot allemand « Alanin », qui fait référence à l’aldéhyde, ou plus précisément à l’acétaldéhyde-ammoniac. Il s’agit du composé chimique à partir duquel ce chercheur a pu isoler l’acide aminé. (1)
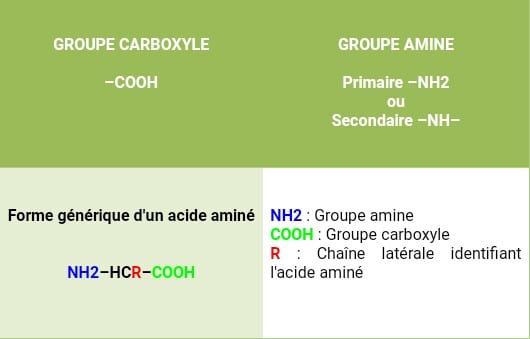
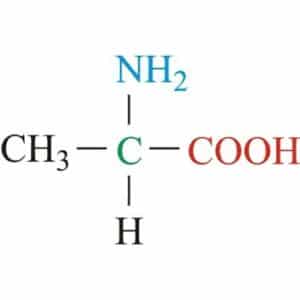
Cet acide aminé a pour formule chimique C3 H7 NO2 et masse molaire 89,0932 g/mol. Il fait partie de ce que l’on appelle en biochimie, « acide aminé aliphatique non polaire ». Car la chaine latérale (R) attachée au carbone α (Cα) est un groupe méthyle non réactif (–CH3), n’ayant que très peu de rôles à jouer dans les fonctions protéiques. Il renferme aussi un groupe α-aminé (–NH3+) et un groupe acide α-carboxylique (–COO-). L’alanine présente donc une structure très simple, à l’instar de la glycine. (2)
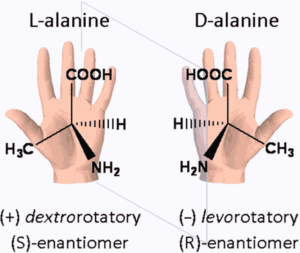
Cet acide α-aminé possède deux énantiomères, à savoir S ou L(+)-alanine et R ou D(-)-alanine. La forme racémique D-alanine est obtenue à partir de l’énantiomère naturelle L-alanine sous l’effet de l’alanine racémase. C’est une enzyme catalysant une isomérisation dite isomérase.
Propriétés biologiques
C’est l’énantiomère L– qui est synthétisée par l’organisme et est visible dans les aliments, sources de protéines. C’est l’un des acides aminés protéinogènes les plus fréquemment rencontrés, aux côtés de la leucine, en représentant 7,8 % environ de la structure primaire d’un échantillon de 1 150 protéines.
Chez l’Homme comme chez d’autres mammifères, cet acide α-aminé intervient dans le cycle glucose-alanine, également appelé cycle de Cahill. Ce dernier a lieu entre le foie et les tissus de l’organisme, notamment les muscles. C’est une série de réactions au cours desquelles les carbones et les groupes aminés issus de la dégradation des acides aminés au sein des muscles sont transportés vers le foie.
Lorsque les cellules musculaires dégradent les acides aminés pour la production d’énergie, l’azote qui résulte de cette réaction est transaminé en pyruvate et L-glutamate. Sous l’effet de l’enzyme alanine transaminase, ces derniers génèrent de l’α-cétoglutarate et de L-alanine, qui sera transportée via la circulation sanguine afin d’atteindre le foie. Une fois l’alanine arrivée au niveau de cet organe, le pyruvate est régénéré et entre dans le processus de gluconéogenèse afin de former du glucose, essentiel pour les muscles. Le L-glutamate régénéré, de son côté, atteint les mitochondries et subit une autre réaction sous l’effet de l’enzyme déshydrogénase. Ce qui forme alors l’ammonium et l’α-cétoglutarate qui à leur tour entrent dans le cycle de l’urée. (3)
L’isomère D-alanine, de son côté, peut être également rencontré dans la nature, dans les parois cellulaires de certaines bactéries, où il entre dans la synthèse du peptidoglycane. Cette substance n’est autre que le premier constituant de ces dites enveloppes cellulaires. Cette énantiomère est aussi présente dans les carapaces des crustacés et des mollusques.
Principales sources
Comme il a été souvent précisé dans ce dossier, l’organisme est capable de produire de l’alanine. Donc, il n’est pas essentiel de s’en procurer. Les suppléments peuvent toutefois servir pour des fins thérapeutiques. Car soulignons ici que cet acide aminé revêt de pas mal de propriétés médicales.

La plupart des aliments que nous consommons au quotidien apportent une certaine dose de ce composé, que ce soit les légumes, fruits, noix, ou les céréales. Sa concentration demeure toutefois plus élevée dans les viandes et certains végétaux gorgés de protéines.
Ci-après une petite liste des gros apporteurs de cet acide aminé :
– Spiruline, 4 515 mg/100 g ;
– Morue séchée, 3 800 mg/100 g ;
– Levure, 2 300 mg/100 g ;
– Viande de bœuf, 2 471 mg/100 g;
– Veau, 2 071 mg/100 g ;
– Dinde, 1 918 mg/100 g ;
– Champignon blanc séché, 1 900 mg/100 g ;
– Esturgeon, 1 887 mg/100 g ;
– Germe de blé, 1 858 mg/100 g ;
– Graines de tournesol, 1 800 mg/100 g ;
– Poulet, 1 803 mg/100 g ;
– Farine de soja, 1 700 mg/100 g ;
– Persil, 1 500 mg/100 g.
Les besoins journaliers en alanine sont de l’ordre de 500 à 2 000 mg par jour pour un adulte en bonne santé. Cependant, en cas d’exercices physiques intenses, pour les athlètes en particulier ; des doses supplémentaires sont nécessaires pour compléter les acides aminés dégradés et reconstruire rapidement la masse musculaire. D’où l’intérêt de prendre des compléments alimentaires et de la poudre de protéine avant et après les exercices de musculation. Ceci permet maintenir le taux des acides aminés à la normale.
Quels sont les bienfaits de l’alanine ?
S’agit-il d’un régulateur de glycémie ?
Une étude scientifique publiée en 2002 a démontré l’effet bénéfique que peut avoir l’alanine sur le taux de glucose sanguin, ou la glycémie. Au cours de cette expérience in vitro réalisée sur des rongeurs, l’ajout de cet acide aminé a permis de réguler la glycémie. La L-alanine a agi comme un stimulus de la sécrétion d’insuline en présence de glucose au niveau des îlots de Langerhans. Rappelons au passage qu’il y a deux types de cellules dans les îlots de Langerhans du pancréas, dont les cellules α situées à la périphérie qui sécrètent le glucagon et les cellules β, l’insuline.
L’adoption de la technique d’observation utilisant la spectroscopie de résonance magnétique nucléaire (RMN) au cours de l’étude a aussi permis de voir que cet acide aminé a boosté le métabolisme du glucose. Les scientifiques ont conclu que les suppléments en L-alanine peuvent servir à lutter contre l’hypoglycémie, qui risque de causer des dommages irréversibles au cerveau. Il a été aussi constaté que l’amélioration du métabolisme du glucose a conduit à une réduction des symptômes du diabète (4). Bien que les résultats de ces études soient encourageants, ils ne nous permettent pas de conclure sur l’efficacité de cet acide aminé contre cette pathologie. Cet effet reste donc à confirmer chez l’homme.
Est-un protecteur des reins ?
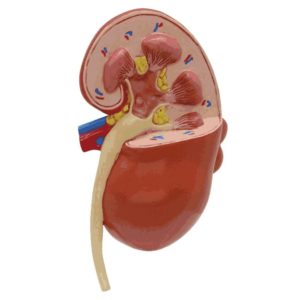
Certains scientifiques ont aussi mis en avant l’action protectrice de cet acide α-aminé vis-à-vis des reins, en réduisant les risques de calculs rénaux, notamment chez les sujets ayant des antécédents familiaux. Au cours de cette étude menée par Walter A. Müller et son équipe, la L-alanine a été injectée chez des chiens en bonne santé, afin de voir son effet précurseur gluconéogénique. On a utilisé une dose de 0,75 mmol/kg de cet acide aminé, pour ce faire.
Ces quelques études cliniques ne sont pas toutefois suffisantes pour conclure sur l’efficacité de cet acide aminé. D’autres études sur l’homme doivent être menées avant de confirmer quoi que ce soit.
– Effet sur le glucagon
Près de 15 minutes après l’injection, les contrôles réalisés ont permis de constater une hausse significative du glucagon pancréatique, de 90 pg/ml environ. L’insuline a aussi augmenté de 8 µg/ml. Une seconde injection après une heure a entrainé une autre hausse du glucagon, allant de 350 pg à 1 066 pg/ml. Les chiens sont ensuite mis à jeun pour voir si cet acide aminé a encore des effets sur la stimulation de ces deux hormones. Les résultats ont montré que la L-alanine a favorisé la synthèse de glucagon, mais a eu peu d’effet sur la sécrétion d’insuline. (5)
Pour l’instant, la plupart des essais cliniques ont été réalisés sur des modèles animaux. Ce qui ne nous permet pas de confirmer la réelle efficacité de ce produit sur l’homme.
– Actions sur les reins
La question qui se pose maintenant est que, en quoi le glucagon peut aider dans la protection des reins ? Cette hormone, dite hormone du besoin énergétique, joue en réalité de nombreux rôles sur la plupart des organes. Elle agit sur le cœur grâce à son effet chronotrope, le foie en stimulant la néoglucogenèse et la glycogénolyse. Au niveau des reins, elle augmente l’excrétion de sodium et de phosphate par les urines. Le glucagon est connu aussi pour améliorer le débit de filtration des glomérules. La stimulation de cette hormone grâce à des suppléments de L-alanine constitue donc une mesure de prévention contre les calculs rénaux et l’insuffisance rénale. (6)
D’autres essais cliniques demeurent toutefois nécessaires avant de confirmer cette qualité thérapeutique.
Cet acide aminé est-il bénéfique pour la prostate ?
Certaines revues scientifiques ont aussi parlé de la capacité de la L-alanine prise en complément alimentaire à lutter contre le cancer de la prostate. Les chercheurs ont, en effet, observé qu’une concentration élevée de cet acide aminé dans le liquide prostatique permet de lutter contre une hyperplasie et une augmentation irrégulière du volume et de la taille de cette glande.
L’utilisation de l’acide aminé chez les sujets expérimentés a entraîné une réduction des douleurs et des problèmes de miction, du gonflement des tissus de la glande, et des risques d’une évolution vers un cancer de la prostate. Pas mal de médecins étrangers ont recours à cet acide aminé pour traiter le cas d’hyperplasie prostatique et de cancer de la prostate, d’après la même publication scientifique (7). Il faut plus d’études cliniques toutefois avant de confirmer ces propriétés.
Quels sont ses autres bienfaits sur la santé ?
Les essais cliniques qui prouvent les autres bienfaits de l’alanine, sur la santé, manquent malheureusement. Il est connu que cet acide aminé entre dans la synthèse de globules blancs et est donc indiqué pour booster le système immunitaire en cas d’infection, ou de maladies. Certains ouvrages scientifiques ont aussi parlé de son rôle de neurotransmetteur et de ses effets bénéfiques pour le cerveau. Il semblerait qu’il améliore le fonctionnement de cet organe.
Alanine VS β-alanine

Pour éviter les confusions, il reste judicieux aussi de parler en quelques lignes, de la β-alanine. En biochimie, elle est dite isomère de position de l’α-alanine, autrement dit l’alanine. Leurs différences résident, en effet, au niveau de leurs structures chimiques ; et ce qui change complètement tous ses rôles. La β-alanine fait partie intégrante des acides β-aminé et en tant que tel, son groupe amine se trouve donc en position β et non α, par rapport à son groupe carboxylate. Elle ne possède pas de centre chiral, donc pas d’isomère optique ou d’énantiomère. Ce composé chimique est connu également sous le nom d’acide β-aminopropanoïque.
Ses fonctions physiologiques n’ont rien à voir avec celles de l’alanine. Cet acide β-aminé ne joue aucun rôle dans la synthèse des protéines ou celle d’une enzyme particulière. Sa formation est issue de la dégradation de la carnosine et du dihydrouracile. On le recommande surtout en tant que supplément aux athlètes et ceux qui pratiquent de la musculation, car il décuple la concentration de carnosine dans les tissus musculaires. Or, la carnosine est essentielle en cas d’efforts physiques importants pour réduire rapidement la sensation de douleur et multiplier le travail des muscles. (8)
Bien choisir son alanine en poudre
Prendre de la β-alanine en complément alimentaire est très courant de nos jours, en particulier chez les passionnés de fitness et de musculation, ainsi que les athlètes professionnels. Ce supplément permet d’optimiser ses performances sportives. Mais qu’en est-il de l’alanine ? Est-il nécessaire de s’en procurer compte tenu de son caractère, non essentiel à l’organisme ?
En tant qu’acide aminé non essentiel, l’alanine est toujours synthétisée à des concentrations suffisantes dans notre organisme. Par ailleurs, les aliments que nous consommons au quotidien en apportent à des quantités considérables. Donc, les risques de carence sont minimes, voire nuls. Puisque c’est tout simplement le deuxième acide aminé le plus abondant de notre corps.
La prise de cet acide aminé est toutefois impérative, en particulier à ceux qui s’entrainent durement. La L-alanine prévient la fatigue musculaire, augmente l’endurance physique, contribue à la production d’énergie et aide à la récupération rapide des muscles après les entrainements. Dans le domaine de la santé, ce supplément permet de réguler le niveau de glucose sanguin, booster l’immunité et de bénéficier de tous les bienfaits cités dans les paragraphes précédents. Le choix se portera sur les marques connues pour la qualité de leurs produits, et toujours sur la forme naturelle L-alanine bioassimilable, l’isomère que l’on trouve naturellement dans les aliments.
Alanine : Quelle est la posologie efficace ?
La dose de L-alanine que nous devons prendre au quotidien est de 500 à 2 000 mg, comme mentionnée précédemment. En cas de supplémentation, le dosage va de 2 g à 6 g par jour, en fonction du poids du corps. Aucune étude scientifique n’a parlé de surdosage car l’organisme arrive à réguler son taux de concentration en alanine naturellement. Ces dosages sont juste donnés à titre informatif. Il reste toujours prudent de suivre les conseils d’un professionnel de santé.
Les femmes enceintes et allaitantes, les sujets ayant des problèmes d’hypoglycémie et de troubles hépatiques doivent impérativement signaler leurs médecins avant d’entamer tout traitement à base de cet acide aminé. Attention, la prise d’un complément alimentaire doit être supervisée par un médecin.
Références
(1) Strecker A. « Ueber einen neuen aus Aldehyd-Ammoniak und Blausäure entstehenden Körper ». (À propos de la nouvelle substance issue de l’acétaldehyde-ammoniac). Annalen der Chemie und Pharmacie. 1854, 91(3):349-351.
(2) Mc Graw Hill Education. Textbook of Biotechnology. 2012.
(3) Naik Pankaja. Essentials of Biochemistry. JP Medical Ltd. November 2011. p168.
(4) Brennan L and al. « A nuclear magnetic resonance-based demonstration of substantial oxidative L-alanine metabolism and L-alanine-enhanced glucose metabolism in a clonal pancreatic beta-cell line : Metabolism of L-alanine is important to the regulation of insulin secretion ». Diabetes, June 2002; 51 (6): 1714-21.
(5) Walter A. Müller and al. « The effect of alanine on glucagon secretion ». J Clin Invest October 1971; 50(10):2215-2218.
(6) Grimaldi A. « Traité de diabétologie, Glucagon ». Paris, Flammarion 2005. pp:67-89.
(7) Shiga H and al. « Treatment of prostatic hyperplasia by amino acid ». 2008. p:625-632.
(8) Hill CA and al. « Influence of β-alanine supplementation on skeletal muscle concentrations and high intensity cycling capacity ». Amino acids vol 32, n°2, 2007, p:225-233.