Synthétisée à des quantités insuffisantes par l’organisme, la cystéine joue un rôle important dans la constitution d’un nombre non négligeable de protéines importantes. Quelles sont ses propriétés médicinales ? A-t-elle des relations avec l’Acétyl-cystéine ? Comment bénéficier de ses bienfaits ? Trouvez dans ce résumé d’études ce que dit la science à son sujet. Attention, ces informations ne sont pas comparables à un avis médical.

La Cystéine est un acide aminé semi-essentiel du fait qu’elle est produite par l’organisme humain, mais à une quantité réduite toutefois. C’est un acide α-aminé « soufré » qui possède deux énantiomères qui sont la L ou R(+)-cystéine et la D ou S(-)-cystéine. Son énantiomère L ou R(+)-cystéine est encodé génétiquement à partir des ARN messagers portant les codons UGU et UGC au niveau des ribosomes dans le cytoplasme des cellules de l’organisme. Après la transcription de l’ARN messager, elle entre dans la constitution des protéines ; c’est pourquoi elle est dite acide aminé protéinogène.
Sommaire
Présentation de la cystéine
Propriétés physiques et chimiques
La cystéine, connue aussi sous d’autres identifications scientifiques, à savoir les abréviations Cys, C et le nom UICPA Acide 2-amino-3-mercapto-propanoïque, a été identifiée par E. Baumann en 1885. Son nom fut tiré de celui de la substance à partir de laquelle elle fut isolée par réaction de réduction : la Cystine. Le nom de cette substance provient du terme grec « kustis », littéralement traduit en français par « Vessie » en faisant référence à certains calculs vésicaux dans lesquels ce composé fut découvert.

Cet acide aminé a pour formule chimique brute C3 H7 NO2 S, avec une masse molaire de 121,158 g/mol. (1)
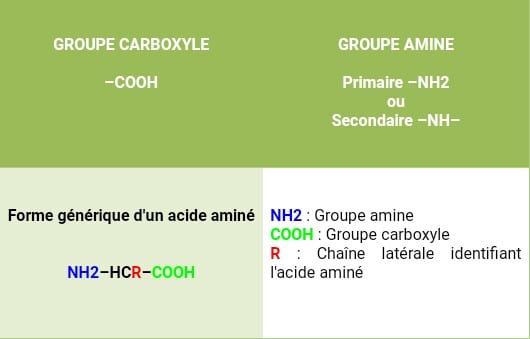
La cystéine possède, comme tout acide aminé un groupement carboxyle –COOH et un élément amine –NH2. Ce qui caractérise la cystéine de ses compères est la présence d’un atome de soufre au niveau de sa chaine latérale, sur un groupe –SH appelé sulfhydryle et qui constitue une fonction thiol. Ce groupement thiol est fragile puisqu’il s’oxyde très facilement mais profère cependant à la cystéine un rôle déterminant dans le métabolisme et dans la structure tertiaire des protéines par la constitution de pont disulfure à l’issue de l’oxydation de deux thiols. (1)
Ses propriétés biologiques
Comme il a été dit, l’énantiomère L- de la cystéine n’est produite dans l’organisme humain qu’en quantité insuffisante ; elle n’est également présente qu’en faible quantité dans la plupart des protéines.
Parmi les protéines synthétisées à partir de cet acide aminé se trouve la mélanine, un pigment colorant l’appareil cutané retrouvé chez l’Homme comme chez d’autres espèces animales et jouant le rôle très important de barrière contre certaines radiations dangereuses des rayons du soleil. Il y a aussi le collagène qui assure l’élasticité et la fermeté de la peau et d’autres tissus de l’organisme, et enfin la kératine qui est l’élément essentiel des fibres capillaires, responsable de leurs solidité et qualité.
Cet acide aminé intervient aussi dans la synthèse du coenzyme A, un coenzyme impliqué dans de nombreuses voies très importantes du métabolisme comme dans le cycle de krebs, également appelé cycle de l’acide citrique. Pour rappel, ce processus biologique se déroule dans les mitochondries des eucaryotes et consiste en une série de réactions biochimiques dont le principal but est d’oxyder des groupes acétyles obtenus à partir des glucides, des graisses et des protéines pour en soutirer de l’énergie sous forme d’électron et de molécule d’adénosine triphosphate ou ATP. Le coenzyme A agit par transfert de groupement acyle et par la formation de thioesters grâce à la liaison de sa fonction thiol avec un groupe carboxyle. La constitution de ces thioesters qui sont particulièrement riches en énergie est une étape importante pour la suite de chacune des réactions biochimiques, car elle permet d’« activer » le composé lié.
Cet acide aminé joue également un rôle important dans le maintien du potentiel redox du cytoplasme cellulaire par sa fonction thiol et par un composé essentiel dont il est le facteur limitant de sa production et l’élément clé de son activité, à savoir le Glutathion. Notons que le glutathion est un pseudo-tripeptide formé à partir de la condensation de glycine, de cystéine et d’acide glutamique. Il constitue un couple d’oxydoréduction très importante dans la cellule. Dans sa forme réduite, le glutathion permet un transfert d’électron et entre en jeu dans l’épuration des agents oxydants et assure ainsi la protection de la cellule contre les radicaux libres, agents impliqués dans le processus de vieillissement cellulaire.
La cystéine intervient aussi dans le processus de détoxication de l’organisme. Son groupe thiol possède une affinité élevée aux cations métalliques libres dans l‘organisme, dont les métaux lourds ou les métalloïdes toxiques, donnant aux composés dérivés de la cystéine une capacité à capturer et à se lier avec ces ions métalliques et permettant ainsi de faciliter leur transport vers les organes épurateurs et leur élimination.
Dégradation et toxicité
La L-cystéine n’est pas toxique en soi, pour l’organisme. Cependant, lorsque cet acide aminé est chauffé à très haute température jusqu’à décomposition complète, il émet des fumées toxiques composées d’oxyde de soufre et d’oxyde d’azote. (2)
Principales sources
La cystéine est synthétisée dans l’organisme par transsulfuration à partir de la sérine et de la méthionine. Cette production est très limitée chez les enfants de bas âges et les sujets âgés. Il est donc nécessaire d’en connaitre les sources dans l’alimentation journalière pour assurer un apport suffisant afin de remédier à une éventuelle carence. Voici une liste des meilleurs apporteurs de cet acide aminé :

– Soja, 638 mg/100 g ;
– Viande bœuf allant de 382 à 460 mg/100 g ;
– Graine de tournesol, 451 mg/100 g ;
– Poulet, 423 mg/100 g ;
– Avoine, 408 mg/100 g ;
– Poisson, 335 mg/100 g ;
– Œufs, 292 mg/100 g ;
– Petit pois, 127 mg/100 g.
Les besoins nécessaires en cystéine sont de l’ordre de 287 mg par jour pour une personne de 70 kg, et plus élevés chez les tout-petits et les sujets âgés. Dans certains cas de pathologie, tels que syndrome de mal absorption intestinale et troubles métaboliques, des apports supplémentaires en cet acide aminé sont essentiels.
Quels sont les bienfaits de la L-cystéine ?
Cet aminoacide a-t-il un effet sur l’hypertension artérielle ?
Des études menées sur la cystéine ont montré que cet acide aminé aurait des effets bénéfiques sur l’hypertension artérielle. Des expériences ont été réalisées sur des rats modifiés génétiquement pour présenter une hypertension. On leur avait administré une certaine dose de cet acide aminé, ce qui a permis d’obtenir une baisse notable de leur pression sanguine.
La L-cystéine entre en synergie avec le glutathion pour augmenter et préserver la biodisponibilité du monoxyde d’azote –NO, un puissant vasodilatateur naturel de l’organisme et protecteur de l’endothélium vasculaire. En effet, ces deux composés agissent d’un côté en tant que puissants réducteurs afin de restaurer le potentiel anti-oxydatif de l’organisme et de protéger le monoxyde d’azote contre une réaction d’oxydation.
D’un autre côté, la liaison du monoxyde d’azote avec le groupe sulfhydryle permet d’obtenir une combinaison plus stable mais prête à se libérer rapidement en cas de besoin par l’organisme. (3)
Utilisé chez l’Homme, cet acide aminé a aussi fait ses preuves en favorisant la baisse de la pression sanguine des sujets hypertendus testés. Ses effets étaient similaires à ceux du Lisinopril, un médicament fréquemment prescrit dans le traitement de l’hypertension artérielle et qui a été, par ailleurs, utilisé auparavant chez ces patients. (4)
Il nous faut d’autres essais cliniques menés sur l’homme avant de pouvoir confirmer ce bienfait. Les quelques études menées sur des animaux de laboratoires ne sont pas en effet suffisantes pour conclure sur l’efficacité de cet acide aminé sur l’hypertension artérielle.
Est-ce un remède pour prévenir la chute des cheveux ?
Des expériences scientifiques ont démontré le rôle de cet acide aminé dans le processus de croissance des cheveux, et notamment dans la prévention de l’alopécie.

Au cours de cette étude à titre d’exemple, des souris ont été exposées à une machine émettant une fumée qui favorise la chute de leurs poils. Afin de découvrir l’effet de ce composé chimique, quelques-uns de ces animaux ont reçu pendant 6 mois de la vitamine B6 additionnée de L-cystéine à raison de 3 fois par jour.
À l’issue de l’expérimentation, il a été remarqué que la perte de poils a été moindre chez les souris soumises à la L-cystéine et à la vitamine B6, comparées au reste du groupe qui n’en a pas reçu. Cet acide aminé agit en tant qu’élément essentiel à la synthèse de kératine, et la vitamine B6 de son côté favorise l’absorption de ce composé par les cellules pilaires. (5)
Chez l’Homme, une étude entreprise par Morganti et son équipe a permis de mettre en évidence l’influence de la L-cystéine sur la croissance des cheveux. L’expérience comptait 48 volontaires d’une tranche d’âge compris entre 21 et 38 ans. Ces derniers ont été invités à utiliser une lotion à base de palmier de Floride ou Serenoa repens en jargon scientifique, pendant le traitement. Seulement, 12 d’entre eux ont pris cependant des suppléments de L-cystéine.
À la fin des 50 semaines de traitement, il a été remarqué chez les individus ayant utilisé uniquement la lotion capillaire une augmentation de 20 % du volume de leurs cheveux. Par contre, ceux qui ont été soumis à un régime enrichi en cystéine ont gagné plus de 50 % du volume initial de leur masse capillaire. (6)
Comme la plupart des observations cliniques ont été menées sur des échantillons d’animaux, il est trop tôt pour conclure sur l’efficacité de cet acide aminé contre la chute capillaire. Il faut d’autres études sur l’homme avant de confirmer cette propriété.
Permet-il de se protéger contre la toxicité des métaux lourds ?
L’effet protecteur de la cystéine vis-à-vis de la neurotoxicité du plomb a été démontré chez l’animal dans une étude menée en 2016. L’expérience consistait à observer l’évolution histologique des tissus nerveux de souris albinos exposées à l’acétate de plomb pendant 7 jours. Une part des animaux testés a reçu de L-cystéine en complément, et une autre n’a rien reçu pour servir de témoins.
L’examen histologique du cortex cérébral, de l’hippocampe et du cervelet de ces souris après l’exposition avait montré une désorganisation tissulaire, des dégénérations ainsi que des pertes neuronales importantes. Les dommages étaient néanmoins beaucoup moins sévères chez les individus traités avec la L-cystéine. (7)
Une tout autre expérience réalisée chez des rats de laboratoire a aussi démontré l’action protectrice de cet acide aminé contre la toxicité aiguë du chlorure de methylmercure. Il a été remarqué que la L-cystéine a réduit la quantité de ce composé chimique cumulé au niveau du cerveau et des reins de ces animaux. (8)
Le manque d’études observationnelles ne permet pas de confirmer la réelle efficacité de cette molécule naturelle chez l’homme. D’autres essais cliniques de plus grande envergure sont essentiels avant de conclure sur cet effet.
A-t-il un effet bénéfique contre les méfaits du tabac ?
Une étude effectuée sur des cellules pulmonaires de hamster en culture a mis en évidence les qualités protectrices de cet acide α-aminé contre les méfaits du tabac. Les cellules expérimentées ont été exposées aux fumées de cigarette et de marijuana pendant plusieurs, avant de recevoir de la L-cystéine. Il a été remarqué que les cellules saines sont devenues malignes à cause de cette intoxication au tabac. Cependant, l’ajout de la L-cystéine a bloqué cette mutation et a permis de protéger les cellules saines restantes. (9)
Pour l’instant, la plupart des essais cliniques ont été réalisés sur des échantillons de cellules. Ce qui ne nous permet pas de confirmer la réelle efficacité de ce produit sur l’homme.
Acétyl-cystéine à ne pas mélanger avec la cystéine
À ne pas confondre avec la L-cystéine, l’acétyl-cystéine est un acide aminé non essentiel qui lui est dérivé. Celui-ci est formé après adjonction d’un groupe acétyl au niveau de son atome d’azote. Il possède également un groupe thiol et par conséquent, la plupart des propriétés biochimiques de la L-cystéine.
En effet, l’acétyl-cystéine, connu sous l’abréviation scientifique NAC ou N-acétylcystéine, a aussi un rôle à jouer dans le processus de détoxification. Il intervient également dans la biosynthèse de glutathion, en stimulant sa production. À part tous ces rôles, cet acide aminé possède bien d’autres propriétés qui lui sont propres et qui sont aussi exploitées dans le domaine médical.
Bien choisir sa cystéine en gélules
La cystéine dans sa forme naturelle est particulièrement difficile à manipuler, car au contact de l’air, elle s’oxyde facilement. Il est possible de trouver des gélules de L-cystéine sur le marché – la forme disponible dans les aliments – mais souvent à des prix élevés ou mélangés à d’autres principes actifs ou encore acides aminés. C’est la raison pour laquelle, la plupart des expériences scientifiques n’utilisent que sa forme dérivée synthétique, la N-acétylcystéine ou bien son précurseur métabolique, la méthionine. Il convient de connaitre que la NAC, une fois dans les reins, est désacétylée et devient de la cystéine. (10)
L-cystéine : Quelle est la posologie efficace ?
La dose journalière recommandée dans le cadre d’une supplémentation en L-cystéine est de 500 à 3 000 mg/jour, à répartir en deux ou trois prises et à prendre de préférence au milieu des repas. Boire beaucoup d’eau, six à huit verres par jour, afin de prévenir les calculs rénaux. Ces dosages sont donnés à titre informatif. Veuillez demander l’avis d’un professionnel avant toute cure.
Sa prise est contre-indiquée chez les diabétiques ainsi que chez les personnes souffrant d’homocystinurie. Pour les sujets ayant des problèmes rénaux ou hépatiques, il est nécessaire de consulter un médecin avant d’entamer un quelconque traitement à base de ce composé chimique. Une supervision médicale est par ailleurs essentielle si vous envisagez de prendre ce complément alimentaire.
Références
(1) Atomic weights of elements 2007. Chem Qmul.
(2) Lewis RJ Sr. « Sax’s dangerous properties of insustrial materials » 11th Edition. Wiley-Interscience, Wiley & Sons, Inc. Hoboken, NJ 2004, p1059.
(3) Cabassi A and al. « Effects of chronic N-acetylcysteine treatment on the actions of peroxynitrite on aortiv vascular reactivity in hypertensive rats. J Hypertens 2001;19:1233-1244.
(4) Suarez C and al. « NAC potentiates the antihypertensive effect of angiotensin converting enzyme inhibitors » Am J Hypertens 1995;8:859.
(5) Francesco D’Agostini ans al. « Chemoprevebtion of smoke-induced alopecia in mice by oiral administration of L-cysteine and vitamin B6 ». Science vol 46, issue 3 June 2006, p:189-198.
(6) Morganti P and al. « Effect of gelatin-cystein and serenoa repens extract on free radicals level and hair growth ». Journal of applied cosmetology.
(7) Mahmoud YI and Sayed SS. Biotech Histochem: 1-6 (2016).
(8) Sugiyama and al. Toho Igakkai Zasshi 22 (1): 78-85 (1975).
(9) Leuchtenberger C. Br J Exp Pathol 58 (6): 625-634 (1977).
(10) Demirkol O and al. « Biologically important thiols in various vegetables and fruits ». J Agric Food Chem, 2004;52:8151-8154.